Educare le nostre cellule killer a riconoscere, con tecniche di ingegneria molecolare, le cellule tumorali e a distruggerle.
Le cellule CAR-T rappresentano la nuova realtà dell’immunoterapia contro le neoplasie.
L’acronimo CAR-T deriva dall’inglese Chimeric Antigen Receptor T-cell, cellule ingegnerizzate e geneticamente modificate al fine di poter riconoscere bersagli di superficie espressi dalle cellule tumorali. Esse rappresentano una nuova realtà terapeutica non disponibile precedentemente per il trattamento delle neoplasie ematologiche e molto diversa dalla chemioimmunoterapia e/o radioterapia convenzionali.
Le CAR-T sono state recentemente approvate dalla FDA (agenzia regolatoria dei farmaci degli Stati Uniti) per il trattamento della leucemia acuta linfoblastica recidivata/refrattaria e del linfoma non Hodgkin aggressivo a larghe cellule B.
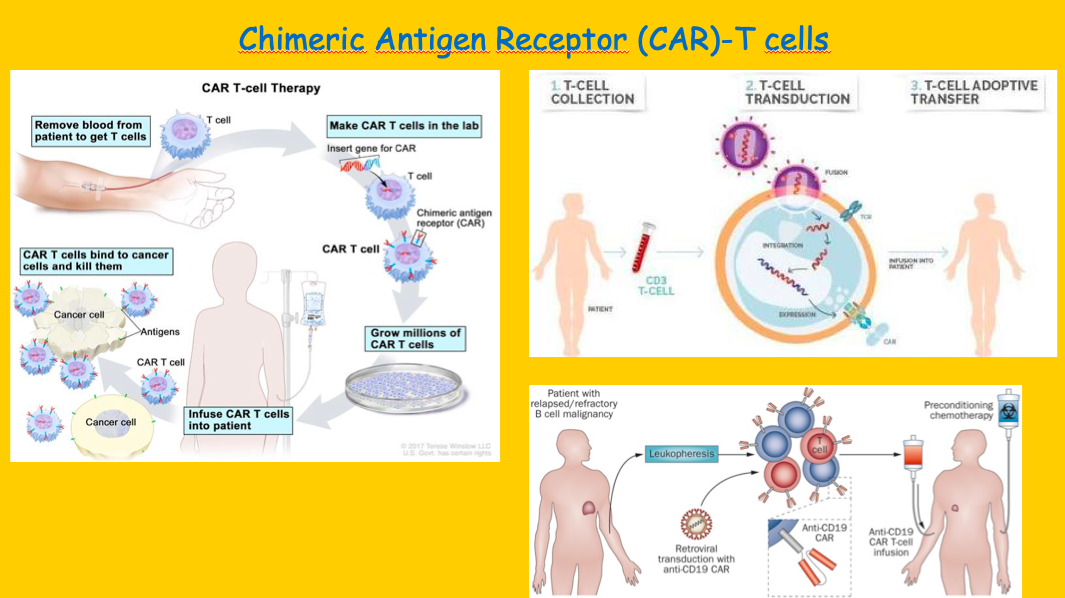
Le cellule CAR-T sono cellule T che vengono prelevate dal paziente e ingegnerizzate in laboratorio al fine di poter riconoscere bersagli predefiniti espressi sulle cellule tumorali. Il bersaglio contro cui tali cellule sono rivolte deve essere espresso selettivamente dalle cellule tumorali e non dalle cellule sane, al fine di poter ottenere il massimo effetto terapeutico minimizzando gli effetti collaterali. Le prime cellule CAR-T sono state ingegnerizzate contro la proteina CD19, espressa sulle cellule B del sistema immunitario così come sulle cellule tumorali di leucemie acute a cellule B e linfomi non Hodgkin aggressivi a cellule B.
Il procedimento terapeutico consiste nel prelevare tramite leucaferesi (tecnica che permette di sottrarre globuli bianchi dal sangue) le cellule T, selezionarle, ingegnerizzarle contro il bersaglio espresso dalle cellule tumorali, attivarle ed espanderle e infine reinfonderle una volte modificate nel paziente. Una chemioterapia immunosoppressiva viene somministrata prima dell’infusione delle cellule CAR-T, le quali, una volta infuse nel paziente, stimolano la produzione di sostanze chiamate citochine in grado di indurre a loro volta l’espansione e la proliferazione delle cellule CAR-T stesse.
A seguito del successo degli studi clinici sulle CAR-T anti CD19, nel 2017 e 2018 Tisagenlecleucel (KYMRIAH) è stato approvato dalla FDA per il trattamento delle leucemie acute linfoblastiche B (LLA-B) recidivate/refrattarie dei bambini e giovani adulti di età < 25 anni e dei linfomi aggressivi a cellule B recidivati/refrattari.
In Italia attualmente il trattamento con Tisagenlecleucel è possibile in studi clinici per i pazienti in età pediatrica o giovani adulti di età < 25 anni affetti da leucemia acuta linfoblastica cellule B e nei pazienti affetti da linfomi aggressivi a cellule B recidivati/refrattari.
Per quanto riguarda la LLA-B recidivata/refrattaria, le cellule CAR-T sono state studiate in diversi trials clinici in cui l’ottenimento della risposta è riportato nel 70-97% dei pazienti. Lo studio capostipite sulle cellule CAR-T è lo studio ELIANA (studio su efficacia e sicurezza dei CAR-T anti CD19 in pazienti affetti da leucemia acuta linfoblastica B recidivata/refrattaria) in cui sono stati trattati 75 pazienti, di cui il 61% già sottoposti a trapianto allogenico di cellule staminali e recidivati post trapianto, con una percentuale cumulativa di risposta del 81%.
Per quanto riguarda invece gli studi clinici sull’utilizzo dei CAR-T anti CD19 nei linfomi aggressivi a cellule B recidivati/refrattari, nello studio capostipite ZUMA-1 in 108 pazienti trattati la riposta globale riportata è stata pari a 82%.
Esattamente come tutte le terapie anti tumorali anche la terapia con le cellule CAR-T è gravata da eventi avversi. I due eventi avversi maggiormente riportati sono la sindrome da rilascio citochinico (CRS) e la tossicità di tipo neurologico.
La CRS insorge generalmente nella prima settimana dopo l’infusione, è indotta da sostanze citochiniche rilasciate massivamente dalle cellule CAR-T e responsabili di una sindrome simil-influenzale caratterizzata da febbre, ipotensione, tachicardia e in alcuni casi insufficienza respiratoria e renale. La CRS è associata a elevati livelli nel sangue di interleuchina-6 e Interferone-gamma, e pertanto il trattamento con Tocilizumab, farmaco anti interleuchina 6, controlla e riduce la gravità di tale evento avverso così come la terapia con cortisonici ad alte dosi.
La tossicità di tipo neurologico può essere invece caratterizzata da cefalea, epilessia, lievi deficit neurologici transitori e risulta rapidamente e completamente reversibile. La causa di tale tipo di tossicità è ancora ad oggi oggetto di studio.
Un altro tipo di tossicità associata alle cellule CAR-T è la distruzione di cellule B sane in circolo, in quanto anch’ esse esprimenti la proteina CD19 in superficie. Questo comporta un maggior rischio di eventi infettivi che viene gestito con terapie di profilassi e infusione di gamma-globuline fino al ripristino delle cellule sane B in circolo.
Nonostante l’indiscussa efficacia, sono stati ad oggi riportati alcuni meccanismi di resistenza che le cellule tumorali sono in grado di sviluppare anche contro le cellule CAR-T. Tali meccanismi sono associati alla perdita dall’espressione della proteina CD19 sulla superficie delle cellule leucemiche. Per tale motivo sono in sviluppo cellule CAR-T in grado di riconoscere multipli target di superficie riducendo così il rischio di possibili resistenze.
Il futuro delle cellule CAR-T riguarda la loro applicazione anche su altre patologie ematologiche recidivate/refrattarie come il mieloma multiplo, la leucemia acuta mieloide, il linfoma di Hodgkin e i linfomi a cellule T.
Un altro campo di applicazione in fase di studio è nei tumori solidi nei quali tuttavia riconoscere un singolo bersaglio tumorale risulta molto più complesso a seguito dell’espressione delle proteine delle cellule tumorali anche su tessuti di organi sani, con conseguente tossicità severa che ne sta limitando ad oggi l’utilizzo.
La terapia con le cellule CAR-T è indubbiamente una nuova strategie terapeutica rivoluzionaria nel trattamento di pazienti con patologie ematologiche aggressive non responsive o recidivate alle terapie di prima e seconda linea e pertanto privi di alternative terapeutiche. Pertanto, seppur gravato da rischi e tossicità non trascurabili, rappresenta un trattamento con indiscusse grandi potenzialità.
Bibliografia:
- Chimeric Antigen Receptor T-Cells: The Future Is Now. Wassim Mchayleh et al, Journal of Clinical Medicine 2019, 8, 207
- Tisagenlecleucel in Children and Young Adults with B-Cell Lymphoblastic Leukemia. Maude S.L et al, NEJM 2018, 378, 439-448
- Chimeric Antigen Receptor Therapy. June CH et al NEJM 2018, 379
- Chimeric Antigen receptor-modified T cells: CD19 and the road beyond. Salter AI et al, Blood 2018, 131, 2621-2629
- Chimeric Antigen Receptor T-Cells for sustained remissions in leukemia. Maude SL et al, NEJM 2014, 371, 1507-1517
- T cells expressing CD19 chimeric antigen receptors for acute lymphoblastic leukemia in children and young adults: a phase 1 dose-escalation trial. Lee D.W. et al, Lancet 2015, 385, 517-528.



